新闻分类
客服中心
尊敬的客户,感谢客户的极大信任,
研诺在偏门认证市场美誉度不断提高,
近期发现市场上有个别人员冒充我司工作人员,
为了维护客户的权益,我司郑重声明:
研诺旗下的三个公司均有“研诺”二字:
深圳研诺信息技术有限公司
东莞研诺技术有限公司
深圳研诺实业有限公司
以上三个公司是研诺的签约主体。任何与以上三个公司不相关的签约主体,如果合同上写着研诺,均为仿冒。敬请留意!
如果您发现以上违规行为,或者如果您需要投拆案件进度与质量,请联系:
总经理:
刘小姐,(86) 13267243767 LIUMEI@YANOTECH.COM
医疗器械在泰国的FDA(Food and Drug Administration)注册,是一个将产品纳入泰国官方监管体系的关键步骤。这个过程旨在确保所有医疗器械在泰国市场的合法销售和使用,从而维护患者和公众的健康安全。
在泰国,医疗器械受到公共卫生部下辖的泰国食品和药物管理局(Thai FDA)的严格监管。无论是本地还是国外的医疗器械制造商,想要将产品引入泰国市场,都必须先通过泰国食品和药物管理局(Thai FDA)的注册程序。这一程序严格遵循泰国相关的法规和法律要求,特别是2019年颁布的新《医疗器械法》和2021年实施的《医疗器械分类法》。
按照新的分类标准,医疗器械根据其风险水平被划分为不同的类别。根据法规B.E. 2562,体外诊断医疗器械和非体外诊断医疗器械均被分为四个风险等级,风险级别从低到高依次为Class 1,Class 2,Class 3,Class 4。
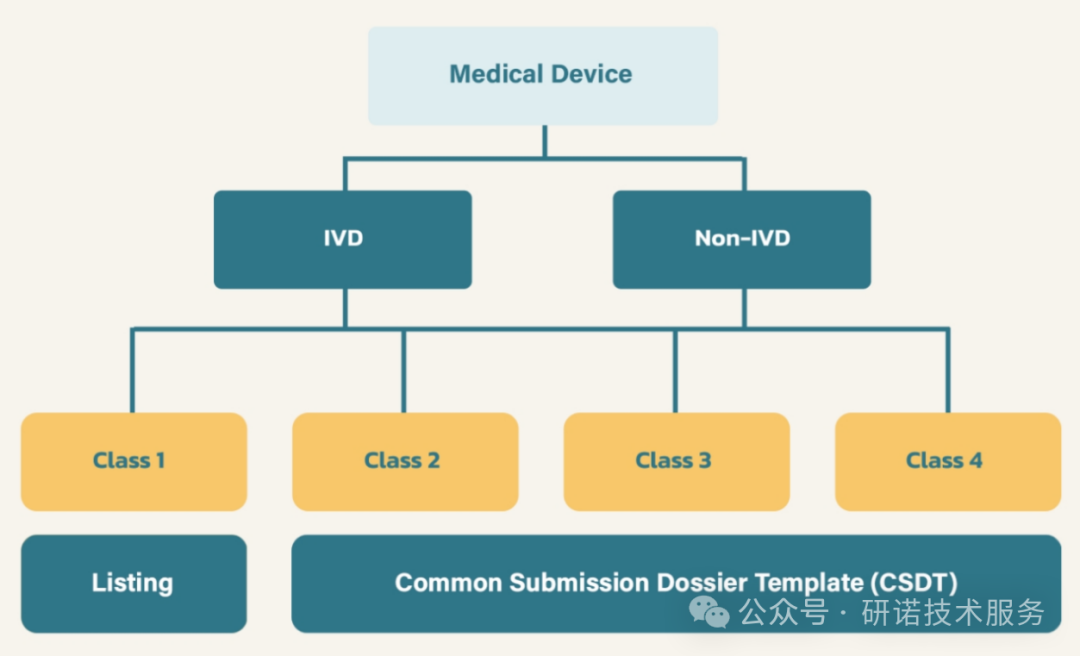
对于不同风险等级的产品,泰国食品和药物管理局(Thai FDA)会采取相应的监管措施。例如,低风险的Class 1产品需要在泰国销售和进口前进行列名;中等风险的Class 2和Class 3产品需进行通知;而高风险的Class 4产品则必须获得泰国FDA的许可证。

了解医疗器械的风险分类只是注册的第一步。根据泰国法规,国外制造商在注册产品之前,必须先在泰国食品和药物管理局(Thai FDA)注册其在泰国的营业场所作为医疗器械的进口商。这一进口商必须是泰国本地注册的公司。这可以通过在国外制造商在泰国设立新公司并获取当地医疗器械许可证,或者委托已有许可证的泰国进口商来实现。无论是新设公司还是委托进口商,都将成为此次注册申请的主体,后续的产品注册也将以其名义进行。
泰国FDA医疗器械注册的一般流程如下:
1)确认产品是否属于医疗器械范畴,并确定其所属的风险类别。
2)国外制造商寻找并授权合适的泰国本地公司作为进口商。
3)准备并提交必要的注册资料给泰国食品和药物管理局(Thai FDA)。
4)泰国食品和药物管理局(Thai FDA)对注册文件进行审核。
5)若文件审批通过,即可获得泰国FDA的注册证书。
在整个注册过程中,制造商可能需要证明其医疗器械的质量体系符合国际标准,如ISO 13485等。对于某些高风险医疗器械,可能还需要进行临床试验以证明其安全性和有效性。此外,医疗器械的标签和包装必须遵守泰国相关法规,包括标明必要的信息、警告和使用说明。
需要注意的是,具体的注册程序和要求可能会因产品特性和法规的更新而有所变化。因此,寻求专业的咨询和团队合作,以确保医疗器械泰国FDA注册的合规性和有效性,是至关重要的。

扫码关注我们
www.yanotech.com













